综合新闻
高小攀副研究员、博士后朱凯祥等在Nature Communications在线发表Sarbecovirus辅助蛋白ORF6抑制天然免疫的分子机制
当前,“受关注的SARS-CoV-2变种病毒”VOCs不断涌现,对全球经济和公共卫生安全带来新一轮挑战。阿尔法(Alpha),德尔塔(delta),奥密克戎(omicron)等VOCs不仅在S蛋白上发生大量突变,突破中和抗体、疫苗的保护作用,而且提高了ORF9b和ORF6等辅助蛋白的mRNA、蛋白质的表达水平,强化了变种病毒抑制天然免疫的能力。
自新冠肺炎疫情爆发以来,病原生物学研究所崔胜团队聚焦冠状病毒入侵、复制及与宿主相互作用的分子机制研究。相继在Acta Pharmaceutica Sinica B(2021,2022);Protein & Cell (2022); Nature Communications(2021)等发表了一系列研究成果。为新冠肺炎疫情的防治提供了重要科技支撑。
2022年8月15日,病原生物学研究所崔胜研究团队和中国科学院生物物理所邓红雨团队在Nature Communications杂志在线发表了题为Structural Basis for Sarbecovirus ORF6 Mediated Blockage of Nucleocytoplasmic Transport的论文。研究人员分别解析了SARS-CoV-2和SARS-CoV ORF6 C-末端片段(CTT)与细胞核孔复合物组分Rae1-Nup98形成的2个复合物晶体结构。进而,他们利用生化、生物物理和细胞功能实验等多种技术揭示了ORF6 阻碍蛋白、mRNA等物质的核孔双向运输以及抑制细胞抗病毒免疫应答的分子机制。
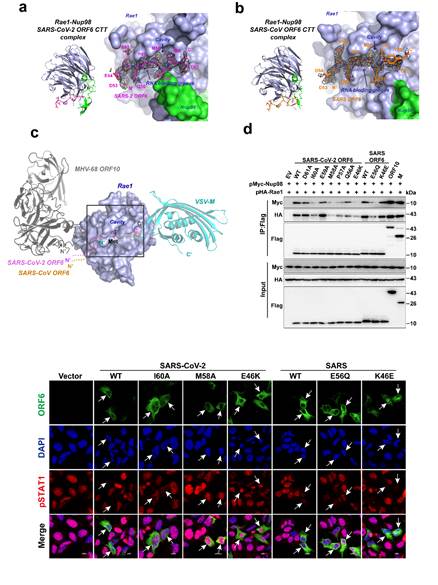
图. SARS-CoV-2/SARS-CoV ORF6 CTT与核孔复合物物组分Rae1-Nup98的复合物晶体结构和功能验证

图. Sarbecovirus辅助蛋白ORF6抑制天然免疫的模式图
中国医学科学院病原生物学研究所崔胜研究员和中国科学院生物物理所邓红雨研究员为本文的共同通讯作者。崔胜课题组副研究员高小攀博士,邓红雨课题组助理研究员田华彬博士以及崔胜课题组博士后朱凯翔为本文的共同第一作者。本研究获得了中国医学科学院医学科技创新工程(2021-I2M-1-037)、科技部国家重点研发计划(2019YFC0840602)、国家自然科学基金(81971985;81772207;81572005;81921005)等项目的资助。
原文链接:https://rdcu.be/cTGDb
